
0.前言
「你們的 IQC 怎麼做?IPQC 多久巡檢一次?FQC 的抽樣標準是什麼?」
這些是採購或研發在評估代工廠時一定會問的問題。在醫材加工這種高精度要求下,品質管理不能只靠最後檢查,重點是讓每一道加工在量產時都維持穩定,不要讓誤差一路累積到成品端。
我們實務上遇過很多案例,問題不是設計錯,而是製程中尺寸慢慢往公差邊界跑,當下沒處理,最後整批才出問題。以骨科產品來說,一顆骨釘如果尺寸超出公差 0.05 mm,就可能影響鎖固效果,甚至增加臨床風險。這類狀況如果等到最後才發現,通常成本已經很高。
因此在委外製造時,除了看最後檢驗結果,也要看代工廠在整個製程中怎麼控管品質。IQC(進料品質控制)、IPQC(製程品質控制)、FQC(成品品質控制)、OQC(出貨品質控制)這四個階段,實際怎麼執行,比制度名稱更重要。
本文從元信豐三十年的加工經驗出發,整理醫材代工在品質管理上的實務做法,並整理評估時可直接使用的查核方向,協助您在專案初期先把風險看清楚。
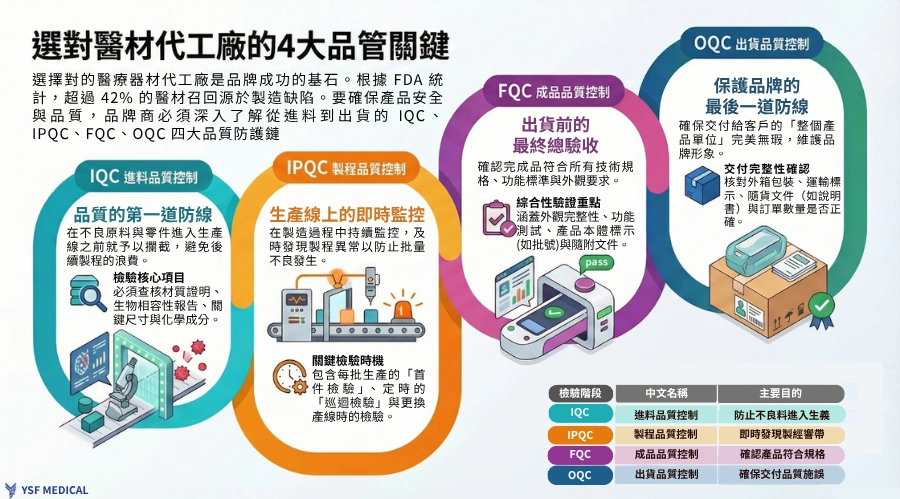
Table of Contents
1.什麼是品質控制(QC)?醫療器材製造的品質管理架構
當您評估一家醫材代工廠時,最先看到的通常是品質控制(Quality Control,簡稱 QC)。但在醫材領域,我們必須釐清QC與品質保證(Quality Assurance,簡稱 QA)的職能差異,才能精準判斷代工廠的穩定性。
1.1 QC vs QA:兩者有什麼不同?
QC(品質控制)就是在各個節點做實際檢驗。包含進料、製程中、成品完成後的量測與檢查。在元信豐現場,QC 會使用校驗過的量具做檢測,例如螺紋塞規、環規、PIN 規量測孔徑,或用顯微鏡檢查毛邊與刀痕,確認零件符合圖面公差要求。
QA(品質保證)看的層面不一樣。QA 不是只看這一件有沒有過,而是看這整套製程能不能一直做出合格品。包含製程怎麼設計、文件怎麼控、操作人員怎麼訓練、設備有沒有定期校驗、供應商怎麼管理,這些都屬於 QA。
對品牌商來說,QC 可以看出有沒有把不良品抓出來;QA 才看得出這些問題會不會一直發生。兩個一起看,才能判斷這家代工廠穩不穩。實務上,有經驗的加工廠不會只看檢驗結果,而是會看量測數據的變化。例如尺寸開始往公差邊界靠近時,會先判斷是不是刀具磨耗,再決定要不要補償或換刀,而不是等到尺寸超差才處理。
1.2 醫療器材品質管理的四大檢驗階段
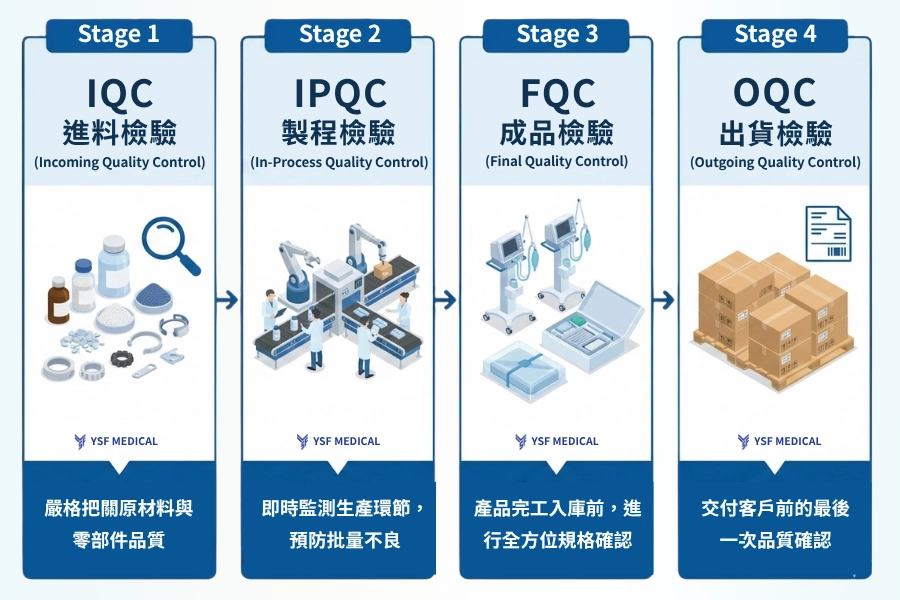
(圖1:IQC/IPQC/FQC/OQC四大檢驗階段流程圖)
醫療器材從原料進廠到成品出貨,必須經過層層品質把關。這套完整的品質控制流程可以用一個簡單的公式來理解:IQC → IPQC → FQC → OQC,形成一道從源頭到終點的品質防護鏈。
| 檢驗階段 | 中文名稱 | 檢驗時機 | 檢驗對象 | 主要目的 |
| IQC | 進料品質控制 | 原物料到廠時 | 原料、零件、包材 | 核對材質證明與料卡,防止不合格原料進入生產線 |
| IPQC | 製程品質控制 | 加工過程中 | 半成品、首件、加工成品 | 即時監控尺寸偏移,及時調整刀具補償,降低批量報廢 |
| FQC | 成品品質控制 | 完工/清洗後 | 成品(包裝前) | 全檢或抽樣確認外觀、尺寸與毛邊符合最終規格 |
| OQC | 出貨品質控制 | 出貨前 | 包裝完成品 | 檢查外觀標示、核對標籤批號與文件,確保交付無誤 |
在實際加工現場,這四個階段的節奏感很重要。IQC 卡住不良棒材、IPQC 攔截製程漂移,不然最後只會一直在收尾、救火。當前端控管做得好,FQC 的工作量會明顯減少,這也是衡量一家代工廠品質系統是否真正落實的間接指標。
1.3 為什麼醫材製造需要更嚴格的品質控制?
與一般工業零件不同,醫療器材的品質管理有其特殊性。這不是法規在刁難,是醫材本身的特性就是這樣:
1.3.1 人命關天,容錯率低
一支骨釘若有微小毛邊或尺寸超差,可能導致鎖固力不足或植入後的感染風險。像這類產品,只要毛邊、尺寸或表面狀況沒有控好,後面的使用風險就會跟著放大,所以加工精度一定要抓得很緊。
1.3.2 法規要求與追溯性
醫材製造需符合 ISO 13485 等規範。這代表每一支產品從原料來源、機台參數到最後的量測記錄,都必須具備完整的可追溯性。對我們而言,這不只是留存記錄,更是對客戶的責任證明。
1.3.3 極高的品質責任風險
醫材召回(Recall)對品牌商的打擊巨大。作為代工夥伴,我們建立嚴謹的 QC 流程,目標就是幫客戶在廠內攔截所有潛在風險,守住產品進入市場前的最後一道防線。
2. IQC 進料品質控制:把關原物料與零組件品質
進料檢驗(IQC)是品質控制的第一道防線,也是最容易被低估的關鍵環節。許多品牌商誤以為只要指定使用符合規格的原料就能確保產品品質,卻忽略了一個事實:即使是同一家供應商、同一批材料證明,實際送達的原料品質仍可能存在差異。
2.1 IQC是什麼?為什麼這麼重要?
IQC(Incoming Quality Control),中文稱為進料品質控制,是指當原物料、零組件、包裝材料送達工廠時在入庫前進行的品質檢驗與判定作業。其核心目的很明確:在不良材料進入生產線之前就予以攔截,避免後續製程的浪費與風險。
我們曾接到客戶緊急來電,詢問為何試產件的螺紋配合出現異常——追溯後發現,棒材批次切換時,外徑公差悄悄漂移了 0.03 mm,但因為 IQC 沒有量測這個項目,直到 IPQC 才發現,導致該批首件全部報廢。這類情況在實務中並不罕見,也是我們後來將棒材外徑列入 IQC 強制量測項目的原因。
在元信豐,我們核對材質證明(CoA)時,不只是對照批號(Lot Number),更會細緻地比對供應商原始標籤、料卡資訊與實際送達材料的一致性。在實務中,我們會特別留意材料的原始狀態,例如:檢查包裝原封條是否完整、材料表面是否有非預期的氧化或存放痕跡。即便是細微的尺寸公差或表面刮痕,在後續 CNC 銑削加工中都可能累積成製程變異;因此,我們在 IQC 階段就落實嚴格的量測與外觀比對,確保進入產線的每一支材料,都具備最穩定的加工基準。
IQC 的價值很直接:在最前面就把問題擋掉,不要讓它進到產線。
2.2 醫療器材IQC的檢驗項目有哪些?
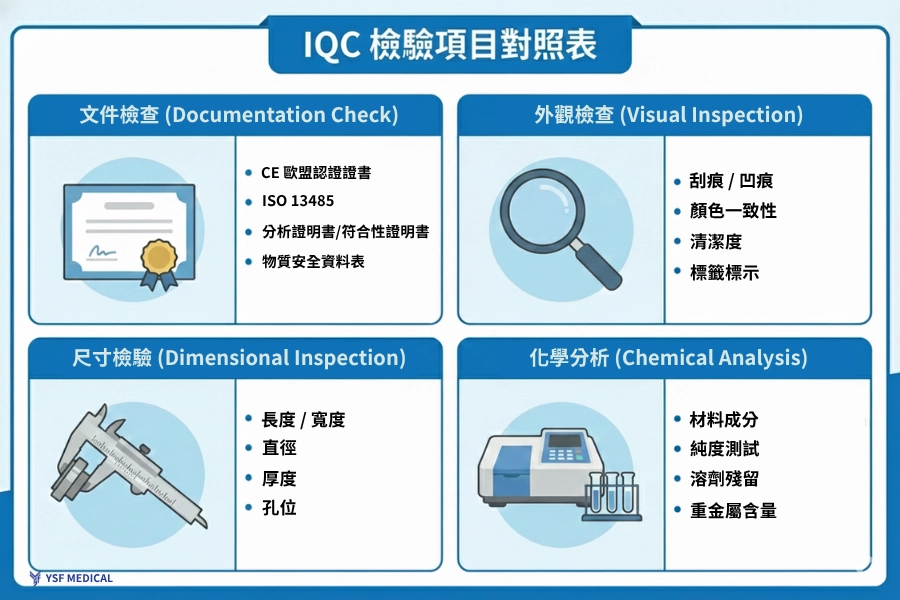
(圖2:IQC檢驗項目對照表)
在醫療器材加工中,IQC 的檢驗項目比一般製造更複雜。除了外觀、尺寸與數量檢查,還要確認材料的法規符合性與追溯性。對精密加工來說,IQC 的細緻度會直接影響後續製程穩定性,因此元信豐特別重視材料的追溯與加工基準一致性,並落實以下四項核心核對:
2.2.1 文件完整性審查:
嚴格確認材質證明(CoA)符合醫材級規範,例如鈦合金 ASTM F136、純鈦 ASTM F67,或是手術器械常用的 630 不鏽鋼(ASTM F899/A564)。我們逐一比對批號是否與送貨單、料卡完全一致,確保化學成分與機械性能皆符合標準。
2.2.2 外觀與包裝檢查:
確認包裝無破損、無受潮,並仔細檢查棒材表面是否有鏽蝕、深層刮痕或異物污染,避免瑕疵進入後續的精密切削程序。 關鍵尺寸量測: 使用經過校驗的精密量具(如分厘卡),確認原料徑向尺寸公差符合加工要求,確保材料上機後的夾持精度與主軸轉速的穩定性。
2.2.3 追溯標記確認:
核對材料端頭或標籤上的原始編號,確保每一支棒材在產線中都能追蹤到其原始熔煉批次(Heat Number),落實醫材法規要求的完整追溯。
2.2.4 關於材質驗證的多元方式:
針對極高風險或有特殊複驗要求的專案,市場上亦有廠商採用光譜儀分析或 XRF 檢測;若客戶有此類精密成分驗證需求,可協助委託具備認證的第三方實驗室(如 SGS)執行,提供最具公信力的數據保障。
3.IPQC 製程品質控制:動態監控變異
在量產過程中,刀具磨損導致的尺寸漂移通常不是突然發生的,而是漸進式的。我們在 IPQC 巡檢中會觀察量測值的趨勢,一旦連續三個樣本往公差邊界靠近,即使還未超出公差,就會觸發刀具補償或換刀評估。如果等到 NG 才處理,通常已經來不及了。提早看到趨勢,才能把損失壓在前面。
3.1 IPQC 的核心價值:預防批量不良
IPQC 是在加工過程中,針對半成品與製程參數進行監控。現場最實際的價值有三個:
3.1.1 防止批量不良發生
透過及時巡檢,能第一時間發現刀具磨損或設備異常導致的尺寸偏移。在發現趨勢異常時立即進行刀具補償或調整,能將生產損失控制在最小範圍內。
3.1.2 確保製程穩定性與可重複性
對醫材零件來說,重點不是某一批做得出來,而是同一套參數換到下一批時,結果還要穩定。透過定期抽檢監控製程是否處於穩定狀態,一旦發現偏移即刻調整。
3.1.3 提供製程改善依據
巡檢累積的數據是分析 製程能力 Cpk 的重要依據,協助技術團隊找出瓶頸工序並優化製程參數。
3.2 IPQC的檢驗時機與頻率
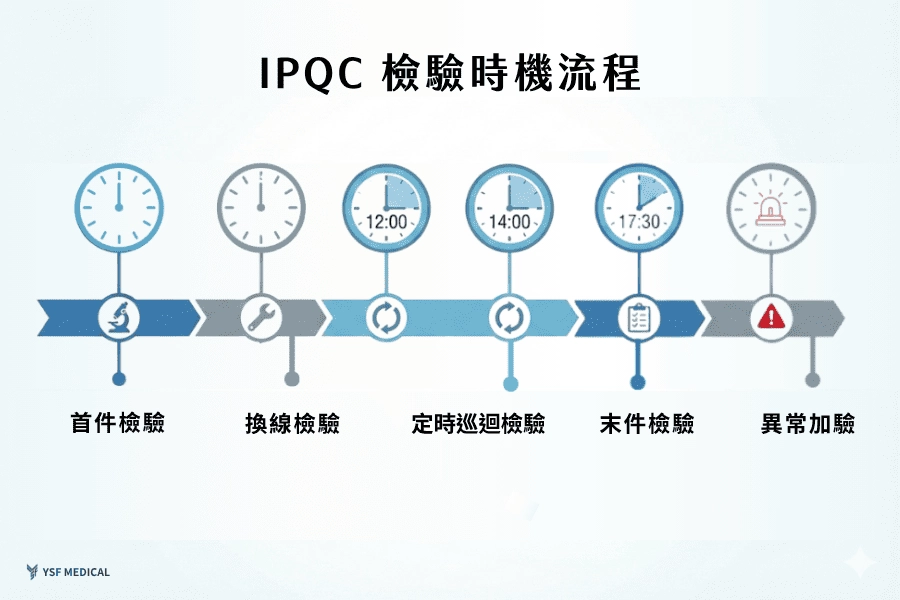
(圖3:IPQC巡檢頻率與時機示意圖)
IPQC檢驗並非隨機進行而是根據製程特性、產品風險、歷史數據規劃出適當的檢驗時機與頻率:
3.2.1 首件檢驗 (FAI, First Article Inspection)
每一批次開工、更換刀具或調整程式後,生產出的前三件產品必須經過全尺寸檢測。只有首件確認符合圖面公差後,機台才會進入量產,確保生產起點沒有問題。
3.2.2 現場操作人員自主抽檢
在量產過程中,機台操作人員需依固定頻率(如每 1 至 2 小時)針對關鍵尺寸進行自主抽檢。這種高頻率的自檢能確保製程在第一線得到最直接的監控。
3.2.3 品保人員定時巡迴檢驗
除了操作員自檢,品保單位亦需進行獨立巡檢抽樣,重點在於趨勢監控。若發現量測值連續接近公差邊界,即使尚未超出公差,也應發出警示並要求調查原因。
3.2.4 異常與停機後的再次抽檢
當製程中發生設備故障、停電復機、人員更換或原料批次切換等異常狀況時,必須額外進行抽檢。此步驟旨在驗證製程恢復後仍處於受控狀態,避免因停機造成的參數變動導致品質瑕疵。
3.3 醫材加工的特殊控管重點
除了尺寸量測,醫材等級的加工更強調以下實務: 材料追溯: 確保每一件半成品都能回溯至原始材料批號與材質證明(MTR)。 刀具管理: 透過顯微鏡觀察切削紋路,預判刀具壽命並先行換刀,避免表面粗糙度(Ra)超出規格。 參數紀錄: 詳實記錄 CNC 轉速、進給量與清洗頻率,確保製程具備可追溯性與穩定度。
4.FQC 成品品質控制:出貨前的最終把關
在完成 IQC 原料控管與 IPQC 製程監控後,產品進入交付前的關鍵階段:FQC 成品品質控制。這一關就是產品做完之後,準備入庫前的最後確認。
4.1 FQC 的定義與最終檢驗的角色
FQC(Final Quality Control)稱為成品品質控制或最終檢驗,是指產品完成所有加工工序後、交付給客戶前的全面檢驗。FQC 的重點,就是確認產品是否符合客戶要求的圖面規格與品質標準。
與監控變異的 IPQC 不同,FQC 側重於「零件總體驗收」。其驗證範疇不限於單一工序的尺寸精度,更涵蓋了表面處理完整性、最終幾何公差以及法規標示的正確性。FQC 就是在確認這批產品交出去時,每一件的狀況都一致,不會到了客戶端才出現落差。
實務案例:FQC 能有效攔截不良品,前提是驗收標準已在專案初期與客戶確認清楚。我們在實務中遇過客戶圖面標示『表面粗糙度 Ra≤0.8』,但未明確指定量測方向,導致同一件產品在雙方量測後結果不同。這類問題若在 FQC 才發現,往往已是交期壓力最大的時刻。建議在打樣階段就建立共同的量測基準與接受條件,才能確保 FQC 結果具備共識基礎。
4.2 FQC的完整檢驗項目清單
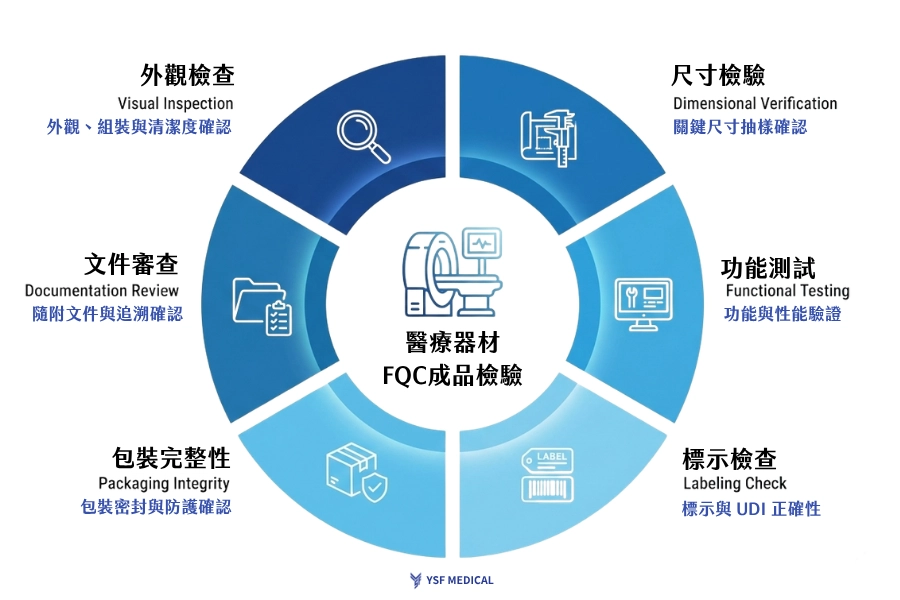
(圖4:FQC成品檢驗流程圖)
4.2.1 外觀完整性與潔淨度
確認表面無加工刮痕、刀痕、鏽蝕或殘留毛邊;檢查無切削油油污或加工碎屑,確保符合後續清洗或滅菌的前提條件。
4.2.2 關鍵品質特性驗證
最終抽樣驗證零件組裝配合面、關鍵功能孔徑或幾何公差(如真圓度、平面度),確認零件在組裝時能正常配合。
4.2.3 功能性配合測試
根據產品特性進行模擬驗證,如螺紋配件的順暢度、鎖定機構的作動測試,確保零件在實際臨床應用中的功能完整。
4.2.4 加工標示正確性檢查
核對產品本體雷射刻字(批號、型號)的準確性、清晰度與耐久性,且標示位置需符合法規要求。
4.2.5 隨附品質文件核對
確認出貨文件齊全,包含詳實記錄實測數據的成品檢驗報告、材質證明等。 追溯標籤或批號卡。
5.OQC 出貨品質控制:最後一道交付防線
在產品完成 FQC 檢驗與妥善防護後,出貨前的最後一關即為 OQC(Outgoing Quality Control)。這一關看的不只是產品本身,而是整批出貨,確認客戶收到的貨品在數量、文件與防護上都沒有問題。
在醫材代工實務中,出貨文件的正確性與零件尺寸同樣重要。批號與材質證明一旦不吻合,不只是行政問題,而是會直接影響客戶端的追溯與法規符合性。我們將 OQC 的文件核對設計為獨立的強制查核步驟,確保每一批出貨的批號、材質證明與成品檢驗報告三方一致,讓客戶在面對稽核時能夠直接取用完整的追溯鏈,不需要事後補件。
5.1 OQC 的定義與核心角色
5.1.1 出貨品質控制的定義
OQC 是指產品進入物流環節前,針對包裝狀態、運輸標示及隨附文件進行的最終抽核,是維護供應鏈信賴度的關鍵。
5.1.2 OQC的檢驗重點與抽樣標準
客戶端的滿意度不僅來自產品精度,更取決於外箱是否完好、文件是否齊全。OQC 確保零件在運輸過程中受到充分保護,避免因物流疏漏造成品牌形象受損。
5.2 OQC的檢驗重點與抽樣標準
OQC的檢驗項目可歸納為四大類:
5.2.1 防護包裝檢查
確認外箱無破損、受潮;檢查內層防護(如泡殼、氣泡袋、防震材)是否牢固,確保精密加工件在運輸過程中不會產生碰撞傷或表面刮損。
5.2.2 交付文件與規格複核
這是 OQC 最核心的任務。核對裝箱單(Packing List)上的型號、數量與實際裝箱是否一致。對於醫材客戶而言,型號或批號一旦錯了,客戶後續的入庫與追溯作業都會受影響。
5.2.3 批號一致性校對
確認產品本體、檢驗報告、材質證明與外箱標籤上的「批號」完全吻合。醫材代工嚴禁混批,若出貨包含多個加工批次,必須確保物理隔離並標示清楚。
5.2.4 運輸標籤與清單核對
核對外箱標籤資訊,包含客戶收貨資訊、訂單編號及總箱數。確保標籤清晰、條碼可辨識,並依需求加註「精密儀器」或「防潮」等運輸警語。
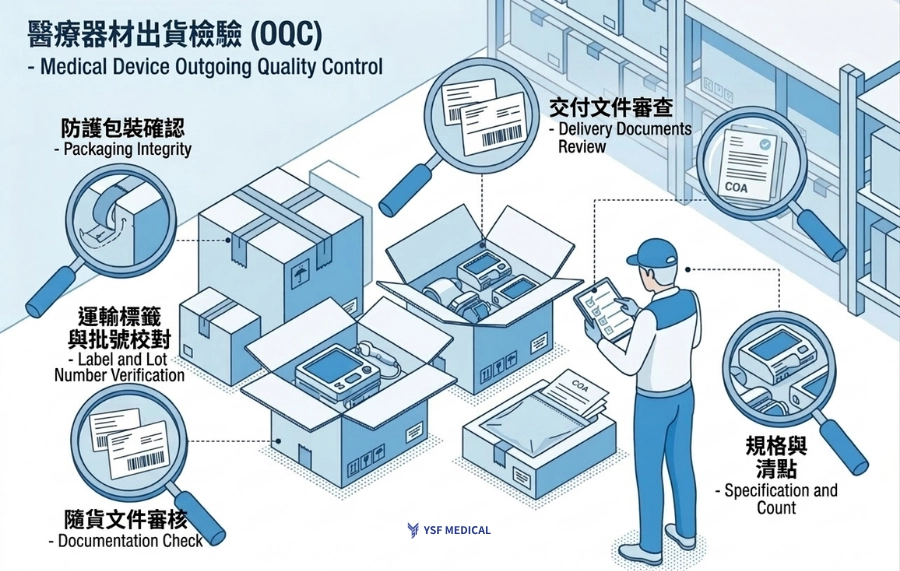
(圖5:OQC出貨檢查重點圖解)
5.3 醫療器材代工的出貨文件與追溯要求
5.3.1 隨貨文件之完整性
確認每批次出貨皆檢附完整文件,包含:
-
裝箱單(Packing List):詳列型號、數量與對應批號。
-
材質證明轉載 (MTR):隨貨附上原始材料商提供的材質成分分析報告。
-
成品檢驗報告(Inspection Report):提供該批次的實測數據。
5.3.2 批號追溯性核對
醫材法規極度重視追溯性。OQC 須確認外箱標示的批號與內部產品、隨貨檢驗報告完全一致,且能精確回溯至製造記錄。
6.醫療器材品質管理的體系支柱
IQC、IPQC、FQC 與 OQC 四道關卡能夠有效運作,背後需要兩個系統支撐:一是提供制度框架的 ISO 13485,二是確保問題不重複發生的 CAPA 機制。少了這兩者,檢驗活動只是各自獨立的把關動作,無法形成真正能持續改善的品質系統。
6.1 ISO 13485:不只是一張證書
ISO 13485 是醫材代工的基本入場資格,但證書本身不等於品質保證。這個標準真正的價值在於它要求工廠將所有影響品質的決策都記錄下來,包含製程參數的設定依據、變更的審核紀錄,以及無法事後驗證的製程(例如精密清洗)必須事先完成確效。 對採購主管而言,評估一家持有 ISO 13485 認證的代工廠時,更值得關注的問題是:他們上一次內部稽核發現了什麼?又怎麼處理? 一家願意誠實回答這個問題的工廠,通常比一家從未出現任何不符合項的工廠更值得信賴,因為前者代表系統真的在運作。
6.2 CAPA:有異常就要一路追到底
CAPA(矯正與預防措施)在實務中常被誤解為「填表格」的行政作業。但它真正的作用是確保同樣的問題不會在下一批、下一個客戶身上重演。 以加工現場為例,當 IPQC 發現某個孔徑尺寸連續三件偏向公差上限,完整的 CAPA 流程不只是換刀具、重新量測,而是追問:是刀具壽命設定不合理,還是切削液濃度在某個時段出現變化?根因找到後,對應的調整必須回寫進 SOP,下一次相同材料、相同工序的加工才能從一開始就避開這個風險。 這種從發現異常、找出根因到更新標準的做法,也是判斷一間代工廠品質系統有沒有真的在運作的關鍵。
Q1.打樣階段是否需要執行完整的 IQC、IPQC、FQC 流程?
打樣階段的核心目的在於規格驗證而非大規模的統計抽樣。由於樣品數量通常較少,重點應放在首件檢驗 (FAI) 與關鍵尺寸的 100% 量測。這些初期的檢驗數據不僅是為了確認打樣合格,更是未來量產時評估製程能力 (Cpk) 的重要基準數據,有助於預判量產風險。
Q2.對於專注研發與行銷的品牌商,我們如何協助落實高品質的製程監控?
我們深知客戶在前端研發的投入,因此在製造端提供完整的數據導向監控機制。除了在合約中明訂具體的檢驗頻率與 AQL 標準外,我們堅持提供具備實際量測數值的檢驗報告,而非僅標註合格。客戶可透過隨時查閱量測儀器的校驗記錄與原始生產日報,確保每一批零件都在受控狀態下生產。
Q3.代工廠具備 ISO 13485 認證,是否代表品質管理絕對可靠?
ISO 13485 證書僅代表工廠建立了符合規定的品質管理系統,屬於基本門檻而非品質保證。評估代工廠的真實執行品質時,應進階審查其內部稽核與不符合項 的改善紀錄。唯有系統能真實反映異常並持續修正,其產出的醫材零件才具備長期穩定性。
Q4.代工過程中發現不良品時,應如何判定責任歸屬?
責任劃分應建立在根因分析 (RCA) 的基礎上。一般而言,製程異常如設備故障或參數設定錯誤由代工廠負責;而設計缺陷如公差設定不合理或材料選用不當則由品牌商承擔。建議在合約中預先約定良率容許上限與補償機制,並透過 CAPA 系統共同尋求改善方案。
Q5.審查代工廠提供的檢驗報告時,有哪些數據真實性的查核要點?
審查報告應首重數據的真實性而非美觀性。真實的製造過程必然存在微小波動,若報告中的量測值過於完美且全數落在公差中心值,通常存在編造風險。應交叉比對儀器校驗日期、生產批號與檢驗員簽章,確保檢驗邏輯的一致性與追溯鏈的完整。
醫材品牌商的成功,關鍵其實就在供應鏈有沒有控好。透過 IQC 進料檢驗、IPQC 製程監控、FQC 成品驗收與 OQC 出貨把關,每一道防線都承載著產品安全與法規合規的重任。品質控管並非獨立的檢驗動作,而是環環相扣的系統化工程。IQC 從源頭阻絕異常材料,IPQC 在加工過程中即時止損,而 FQC 與 OQC 則共同構成交付前的雙重保障。 一個成熟的醫材代工體系,除了擁有 ISO 13485 的系統基礎,更應具備完善的 CAPA 持續改善機制與透明的數據紀錄流程。品質管理不是多花的成本,而是在避免後面更大的風險,也是品牌能不能走得長久的基礎。當品牌商與代工廠把品質評估與監督機制建立起來,製造風險會低很多,產品也比較有機會穩定符合規格。
元信豐專注於醫療器材精密製造超過三十年,我們建立並落實完整的 IQC、IPQC、FQC 與 OQC 品質管理,並通過 ISO 13485 國際認證。我們深刻理解骨科植入物與手術器械對於加工精度、表面處理及生物相容性的嚴苛要求。無論您的產品處於初期開發打樣或正式量產階段,元信豐都能提供符合法規要求的品質管理方案與專業製造建議。 若您對醫材加工品質控管有任何疑問,或正在尋找具備高度合規能力的製造夥伴,歡迎與元信豐聯繫,填寫聯絡表單或來信至 sales@ysfbone.com,我們的團隊將在24小時內與您聯繫提供專業的品質管理解決方案。
10.聲明
本文內容僅供醫療器材產業專業人士參考,所有技術資訊與加工建議皆依公開資料與實務經驗整理,由於實際製造涉及產品特性、使用情境與法規要求,相關決策應由具備資格的技術或法規專業人員進行評估,文中提及之精度數據、加工參數與時程僅為參考值,實際結果仍會因材料、設備與製程條件不同而有所差異。
作者已盡力確保內容的準確性與時效性,但醫療器材產業技術與法規持續演進,部分資訊可能隨時間推移而需要更新,對於因使用本文資訊而產生的任何直接或間接損失,作者不承擔法律責任。
文中案例數據已進行去識別化處理以保護客戶隱私,所有涉及具體產品的描述均已獲得適當授權或改編為通用情境,任何與實際案例的相似之處純屬巧合。
如有任何疑問或需要進一步的技術支援,歡迎透過官方管道聯絡專業團隊進行諮詢。
11.參考資料
American Society for Quality. (n.d.-a). Quality assurance vs quality control.
https://asq.org/quality-resources/quality-assurance-vs-control
International Organization for Standardization. (2016). ISO 13485:2016 medical devices — Quality management systems — Requirements for regulatory purposes.
https://www.iso.org/standard/59752.html
衛生福利部食品藥物管理署. (n.d.-a). 醫療器材委託製造 [Contract manufacturing of medical devices].
https://www.fda.gov.tw/tc/siteContent.aspx?sid=11649
American Society for Quality. (n.d.-b). Process capability.
https://asq.org/quality-resources/process-capability
衛生福利部食品藥物管理署. (n.d.-c). 醫療器材管理 [Medical device management].
https://www.fda.gov.tw/TC/site.aspx?sid=11578&r=83965506
© 2026 元信豐企業股份有限公司 |骨科植入物及手術器材製造專家、ISO 13485 認證醫材廠、CNC 精密加工 |引用或轉載請註明來源,版權所有。
-

設計圖都過了,為何量產卡關?揭示醫材從原型到量產的隱藏風險與DFM實務策略。
-

-

快速打樣加速醫材開發,降低成本並提升精度,助骨科品牌維持創新與競爭力。
-

嚴格品質管理確保骨科植入物安全穩定,保障臨床可靠性。
-

元信豐近日接待元智大學及 7 號演算師生代表,深度探討 AI Agent 於醫療代工製造的應用。透過實地走訪,將課堂理論對接產業實務,並聚焦中小企業導入 AI 的策略、資安與合規架構,共同推進台灣智慧製造人才培育。
.webp) 聯絡我們
聯絡我們

.webp) 聯絡我們
聯絡我們

